തിളച്ചുമറിയുന്നു. ബാഷ്പീകരണത്തിൻ്റെയും കാൻസൻസേഷൻ്റെയും പ്രത്യേക ചൂട്. ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക ചൂട് എന്താണ്, അത് എങ്ങനെ നിർണ്ണയിക്കും
ഈ പാഠത്തിൽ, തിളപ്പിക്കൽ പോലുള്ള ഇത്തരത്തിലുള്ള ബാഷ്പീകരണത്തിലേക്ക് ഞങ്ങൾ ശ്രദ്ധിക്കും, മുമ്പ് ചർച്ച ചെയ്ത ബാഷ്പീകരണ പ്രക്രിയയിൽ നിന്നുള്ള വ്യത്യാസങ്ങൾ ചർച്ചചെയ്യും, തിളയ്ക്കുന്ന താപനില പോലുള്ള ഒരു മൂല്യം അവതരിപ്പിക്കുകയും അത് എന്താണ് ആശ്രയിക്കുന്നതെന്ന് ചർച്ച ചെയ്യുകയും ചെയ്യും. പാഠത്തിൻ്റെ അവസാനം, ബാഷ്പീകരണ പ്രക്രിയയെ വിവരിക്കുന്ന വളരെ പ്രധാനപ്പെട്ട ഒരു അളവ് ഞങ്ങൾ അവതരിപ്പിക്കും - ബാഷ്പീകരണത്തിൻ്റെയും കാൻസൻസേഷൻ്റെയും പ്രത്യേക ചൂട്.
വിഷയം: ദ്രവ്യത്തിൻ്റെ മൊത്തം അവസ്ഥകൾ
പാഠം: തിളപ്പിക്കൽ. ആപേക്ഷിക താപംബാഷ്പീകരണവും കാൻസൻസേഷനും
അവസാന പാഠത്തിൽ, നീരാവി രൂപീകരണത്തിൻ്റെ ഒരു തരം - ബാഷ്പീകരണം - ഞങ്ങൾ ഇതിനകം നോക്കുകയും ഈ പ്രക്രിയയുടെ സവിശേഷതകൾ എടുത്തുകാണിക്കുകയും ചെയ്തു. ഇന്ന് നമ്മൾ ഇത്തരത്തിലുള്ള ബാഷ്പീകരണം, തിളപ്പിക്കൽ പ്രക്രിയ എന്നിവയെക്കുറിച്ച് ചർച്ച ചെയ്യും, കൂടാതെ ബാഷ്പീകരണ പ്രക്രിയയെ സംഖ്യാപരമായി ചിത്രീകരിക്കുന്ന ഒരു മൂല്യം അവതരിപ്പിക്കും - ബാഷ്പീകരണത്തിൻ്റെയും ഘനീഭവിക്കുന്നതിൻ്റെയും പ്രത്യേക ചൂട്.
നിർവ്വചനം.തിളച്ചുമറിയുന്നു(ചിത്രം 1) ഒരു ദ്രാവകത്തെ വാതകാവസ്ഥയിലേക്ക് തീവ്രമായി പരിവർത്തനം ചെയ്യുന്ന പ്രക്രിയയാണ്, നീരാവി കുമിളകൾ രൂപപ്പെടുകയും ദ്രാവകത്തിൻ്റെ മുഴുവൻ അളവിലും ഒരു നിശ്ചിത താപനിലയിൽ സംഭവിക്കുകയും ചെയ്യുന്നു, ഇതിനെ തിളയ്ക്കുന്ന പോയിൻ്റ് എന്ന് വിളിക്കുന്നു.
രണ്ട് തരം ബാഷ്പീകരണത്തെ നമുക്ക് പരസ്പരം താരതമ്യം ചെയ്യാം. തിളപ്പിക്കൽ പ്രക്രിയ ബാഷ്പീകരണ പ്രക്രിയയേക്കാൾ തീവ്രമാണ്. കൂടാതെ, നമ്മൾ ഓർക്കുന്നതുപോലെ, ബാഷ്പീകരണ പ്രക്രിയ ദ്രവണാങ്കത്തിന് മുകളിലുള്ള ഏത് താപനിലയിലും സംഭവിക്കുന്നു, തിളപ്പിക്കൽ പ്രക്രിയ ഒരു നിശ്ചിത താപനിലയിൽ കർശനമായി നടക്കുന്നു, ഇത് ഓരോ പദാർത്ഥത്തിനും വ്യത്യസ്തമാണ്, അതിനെ തിളപ്പിക്കൽ പോയിൻ്റ് എന്ന് വിളിക്കുന്നു. കൂടെ മാത്രമേ ബാഷ്പീകരണം സംഭവിക്കുകയുള്ളൂ എന്നതും ശ്രദ്ധിക്കേണ്ടതാണ് സ്വതന്ത്ര ഉപരിതലംലിക്വിഡ്, അതായത് ചുറ്റുമുള്ള വാതകങ്ങളിൽ നിന്നും തിളയ്ക്കുന്ന ഭാഗത്ത് നിന്ന് - മുഴുവൻ വോള്യത്തിൽ നിന്നും ഒരേസമയം.
ചുട്ടുതിളക്കുന്ന പ്രക്രിയയെക്കുറിച്ച് നമുക്ക് കൂടുതൽ വിശദമായി നോക്കാം. നമ്മളിൽ പലരും ആവർത്തിച്ച് നേരിട്ട ഒരു സാഹചര്യം സങ്കൽപ്പിക്കുക - ഒരു പ്രത്യേക പാത്രത്തിൽ ചൂടാക്കുകയും തിളയ്ക്കുകയും ചെയ്യുന്ന വെള്ളം, ഉദാഹരണത്തിന്, ഒരു എണ്ന. ചൂടാക്കൽ സമയത്ത്, ഒരു നിശ്ചിത അളവിലുള്ള താപം വെള്ളത്തിലേക്ക് കൈമാറ്റം ചെയ്യപ്പെടും, അത് അതിൻ്റെ ആന്തരിക ഊർജ്ജം വർദ്ധിപ്പിക്കുകയും തന്മാത്രാ ചലനത്തിൻ്റെ പ്രവർത്തനത്തിൽ വർദ്ധനവുണ്ടാക്കുകയും ചെയ്യും. ഈ പ്രക്രിയ ഒരു നിശ്ചിത ഘട്ടം വരെ തുടരും, തന്മാത്രാ ചലനത്തിൻ്റെ ഊർജ്ജം തിളച്ചു തുടങ്ങുന്നത് വരെ.
ജലത്തിൽ അലിഞ്ഞുചേർന്ന വാതകങ്ങൾ (അല്ലെങ്കിൽ മറ്റ് മാലിന്യങ്ങൾ) അടങ്ങിയിരിക്കുന്നു, അത് അതിൻ്റെ ഘടനയിൽ പുറത്തുവിടുന്നു, ഇത് ബാഷ്പീകരണ കേന്ദ്രങ്ങൾ എന്ന് വിളിക്കപ്പെടുന്ന സംഭവത്തിലേക്ക് നയിക്കുന്നു. അതായത്, ഈ കേന്ദ്രങ്ങളിലാണ് നീരാവി പുറത്തുവരാൻ തുടങ്ങുന്നത്, കൂടാതെ തിളപ്പിക്കുമ്പോൾ നിരീക്ഷിക്കപ്പെടുന്ന വെള്ളത്തിൻ്റെ മുഴുവൻ അളവിലും കുമിളകൾ രൂപം കൊള്ളുന്നു. ഈ കുമിളകളിൽ വായു അടങ്ങിയിട്ടില്ലെന്ന് മനസ്സിലാക്കേണ്ടത് പ്രധാനമാണ്, മറിച്ച് തിളപ്പിക്കുമ്പോൾ ഉണ്ടാകുന്ന നീരാവിയാണ്. കുമിളകളുടെ രൂപീകരണത്തിനു ശേഷം, അവയിൽ നീരാവിയുടെ അളവ് വർദ്ധിക്കുന്നു, അവ വലിപ്പം വർദ്ധിപ്പിക്കാൻ തുടങ്ങുന്നു. പലപ്പോഴും, കുമിളകൾ തുടക്കത്തിൽ പാത്രത്തിൻ്റെ മതിലുകൾക്ക് സമീപം രൂപം കൊള്ളുന്നു, ഉടനെ ഉപരിതലത്തിലേക്ക് ഉയരുന്നില്ല; ആദ്യം, വലുപ്പം വർദ്ധിക്കുന്നു, അവ ആർക്കിമിഡീസിൻ്റെ വർദ്ധിച്ചുവരുന്ന ശക്തിയുടെ സ്വാധീനത്തിലാണ്, തുടർന്ന് അവ മതിലിൽ നിന്ന് പിരിഞ്ഞ് ഉപരിതലത്തിലേക്ക് ഉയരുന്നു, അവിടെ അവ പൊട്ടിച്ച് നീരാവിയുടെ ഒരു ഭാഗം പുറത്തുവിടുന്നു.
എല്ലാ നീരാവി കുമിളകളും ഉടനടി ജലത്തിൻ്റെ സ്വതന്ത്ര ഉപരിതലത്തിൽ എത്തുന്നില്ല എന്നത് ശ്രദ്ധിക്കേണ്ടതാണ്. തിളയ്ക്കുന്ന പ്രക്രിയയുടെ തുടക്കത്തിൽ, വെള്ളം ഇതുവരെ തുല്യമായി ചൂടാക്കിയിട്ടില്ല, കൂടാതെ താപ കൈമാറ്റ പ്രക്രിയ നേരിട്ട് സംഭവിക്കുന്ന താഴത്തെ പാളികൾ, സംവഹന പ്രക്രിയ കണക്കിലെടുക്കുമ്പോൾ പോലും മുകളിലെതിനേക്കാൾ ചൂടാണ്. ജലത്തിൻ്റെ സ്വതന്ത്രമായ ഉപരിതലത്തിൽ എത്തുന്നതിനുമുമ്പ് ഉപരിതല പിരിമുറുക്കത്തിൻ്റെ പ്രതിഭാസം കാരണം താഴെ നിന്ന് ഉയരുന്ന നീരാവി കുമിളകൾ തകരുന്നു എന്ന വസ്തുതയിലേക്ക് ഇത് നയിക്കുന്നു. ഈ സാഹചര്യത്തിൽ, കുമിളകൾക്കുള്ളിലെ നീരാവി വെള്ളത്തിലേക്ക് കടന്നുപോകുന്നു, അതുവഴി കൂടുതൽ ചൂടാക്കുകയും മുഴുവൻ വോള്യത്തിലുടനീളം വെള്ളം ഏകീകൃത ചൂടാക്കൽ പ്രക്രിയ ത്വരിതപ്പെടുത്തുകയും ചെയ്യുന്നു. തൽഫലമായി, വെള്ളം ഏതാണ്ട് തുല്യമായി ചൂടാകുമ്പോൾ, മിക്കവാറും എല്ലാ നീരാവി കുമിളകളും ജലത്തിൻ്റെ ഉപരിതലത്തിൽ എത്താൻ തുടങ്ങുകയും തീവ്രമായ നീരാവി രൂപീകരണ പ്രക്രിയ ആരംഭിക്കുകയും ചെയ്യുന്നു.
ദ്രാവകത്തിലേക്കുള്ള താപ വിതരണത്തിൻ്റെ തീവ്രത വർദ്ധിപ്പിച്ചാലും തിളപ്പിക്കൽ പ്രക്രിയ നടക്കുന്ന താപനില മാറ്റമില്ലാതെ തുടരുന്നു എന്ന വസ്തുത ഹൈലൈറ്റ് ചെയ്യേണ്ടത് പ്രധാനമാണ്. ലളിതമായ വാക്കുകളിൽ, തിളയ്ക്കുന്ന പ്രക്രിയയിൽ നിങ്ങൾ ഒരു പാൻ വെള്ളം ചൂടാക്കുന്ന ഒരു ബർണറിൽ വാതകം ചേർക്കുകയാണെങ്കിൽ, ഇത് തിളപ്പിക്കുന്നതിൻ്റെ തീവ്രത വർദ്ധിപ്പിക്കുന്നതിലേക്ക് നയിക്കും, അല്ലാതെ ദ്രാവകത്തിൻ്റെ താപനിലയിൽ വർദ്ധനവുണ്ടാകില്ല. തിളയ്ക്കുന്ന പ്രക്രിയയെക്കുറിച്ച് കൂടുതൽ ഗൗരവമായി പരിശോധിക്കുകയാണെങ്കിൽ, ചുട്ടുതിളക്കുന്ന സ്ഥലത്തിന് മുകളിൽ ചൂടാക്കാൻ കഴിയുന്ന പ്രദേശങ്ങൾ വെള്ളത്തിൽ പ്രത്യക്ഷപ്പെടുന്നു എന്നത് ശ്രദ്ധിക്കേണ്ടതാണ്, എന്നാൽ അത്തരം അമിത ചൂടാക്കലിൻ്റെ അളവ്, ചട്ടം പോലെ, ഒന്നോ രണ്ടോ ഡിഗ്രിയിൽ കവിയരുത്. ദ്രാവകത്തിൻ്റെ മൊത്തം അളവിൽ അപ്രധാനമാണ്. സാധാരണ മർദ്ദത്തിൽ ജലത്തിൻ്റെ തിളനില 100 ഡിഗ്രി സെൽഷ്യസാണ്.
തിളയ്ക്കുന്ന വെള്ളത്തിൻ്റെ പ്രക്രിയയിൽ, അത് സീതിംഗ് എന്ന് വിളിക്കപ്പെടുന്ന സ്വഭാവസവിശേഷതകളോടൊപ്പമുണ്ടെന്ന് നിങ്ങൾക്ക് കാണാൻ കഴിയും. നീരാവി കുമിളകളുടെ തകർച്ചയുടെ വിവരിച്ച പ്രക്രിയ കാരണം ഈ ശബ്ദങ്ങൾ കൃത്യമായി ഉണ്ടാകുന്നു.
മറ്റ് ദ്രാവകങ്ങളുടെ തിളപ്പിക്കൽ പ്രക്രിയകൾ വെള്ളം തിളപ്പിക്കുന്നതിന് സമാനമായി തുടരുന്നു. ഈ പ്രക്രിയകളിലെ പ്രധാന വ്യത്യാസം പദാർത്ഥങ്ങളുടെ വ്യത്യസ്ത തിളയ്ക്കുന്ന താപനിലയാണ്, സാധാരണ അന്തരീക്ഷമർദ്ദത്തിൽ ഇതിനകം തന്നെ ടാബ്ലർ മൂല്യങ്ങൾ അളക്കുന്നു. ഈ താപനിലകളുടെ പ്രധാന മൂല്യങ്ങൾ ഞങ്ങൾ പട്ടികയിൽ സൂചിപ്പിക്കുന്നു.
രസകരമായ ഒരു വസ്തുത, ദ്രാവകങ്ങളുടെ തിളയ്ക്കുന്ന പോയിൻ്റ് അന്തരീക്ഷമർദ്ദത്തിൻ്റെ മൂല്യത്തെ ആശ്രയിച്ചിരിക്കുന്നു, അതിനാലാണ് പട്ടികയിലെ എല്ലാ മൂല്യങ്ങളും സാധാരണ അന്തരീക്ഷമർദ്ദത്തിൽ നൽകിയിരിക്കുന്നതെന്ന് ഞങ്ങൾ സൂചിപ്പിച്ചു. വായു മർദ്ദം വർദ്ധിക്കുമ്പോൾ, ദ്രാവകത്തിൻ്റെ തിളപ്പിക്കൽ പോയിൻ്റും വർദ്ധിക്കുന്നു; അത് കുറയുമ്പോൾ, നേരെമറിച്ച്, അത് കുറയുന്നു.
മർദ്ദത്തിൽ ചുട്ടുതിളക്കുന്ന താപനിലയുടെ ഈ ആശ്രിതത്വത്തെ ആശ്രയിച്ചിരിക്കുന്നു പരിസ്ഥിതിപ്രഷർ കുക്കർ (ചിത്രം 2) പോലെ അറിയപ്പെടുന്ന അടുക്കള ഉപകരണത്തിൻ്റെ പ്രവർത്തന തത്വത്തെ അടിസ്ഥാനമാക്കി. ഇത് ഒരു ഇറുകിയ-ഫിറ്റിംഗ് ലിഡ് ഉള്ള ഒരു പാൻ ആണ്, അതിനടിയിൽ, വെള്ളം ആവികൊള്ളുന്ന പ്രക്രിയയിൽ, നീരാവി ഉപയോഗിച്ച് വായു മർദ്ദം 2 അന്തരീക്ഷമർദ്ദം വരെ എത്തുന്നു, ഇത് അതിലെ ജലത്തിൻ്റെ തിളപ്പിക്കൽ പോയിൻ്റ് വർദ്ധിക്കുന്നതിലേക്ക് നയിക്കുന്നു. ഇക്കാരണത്താൽ, അതിലെ വെള്ളവും ഭക്ഷണവും സാധാരണയേക്കാൾ ഉയർന്ന താപനില വരെ ചൂടാക്കാനുള്ള അവസരമുണ്ട് (), പാചക പ്രക്രിയ ത്വരിതപ്പെടുത്തുന്നു. ഈ പ്രഭാവം കാരണം, ഉപകരണത്തിന് അതിൻ്റെ പേര് ലഭിച്ചു.

അരി. 2. പ്രഷർ കുക്കർ ()
അന്തരീക്ഷമർദ്ദം കുറയുന്ന ഒരു ദ്രാവകത്തിൻ്റെ തിളപ്പിക്കൽ പോയിൻ്റ് കുറയുന്ന സാഹചര്യത്തിനും ജീവിതത്തിൽ നിന്ന് ഒരു ഉദാഹരണമുണ്ട്, പക്ഷേ പലർക്കും ദൈനംദിനമല്ല. ഉയർന്ന പർവതപ്രദേശങ്ങളിലെ മലകയറ്റക്കാരുടെ യാത്രയ്ക്ക് ഈ ഉദാഹരണം ബാധകമാണ്. 3000-5000 മീറ്റർ ഉയരത്തിൽ സ്ഥിതി ചെയ്യുന്ന പ്രദേശങ്ങളിൽ, അന്തരീക്ഷമർദ്ദം കുറയുന്നതിനാൽ ജലത്തിൻ്റെ ചുട്ടുതിളക്കുന്ന പോയിൻ്റ് താഴ്ന്ന മൂല്യങ്ങളിലേക്ക് ചുരുങ്ങുന്നു, ഇത് വർദ്ധനവിൽ ഭക്ഷണം തയ്യാറാക്കുമ്പോൾ ബുദ്ധിമുട്ടുകൾക്ക് കാരണമാകുന്നു, കാരണം ഫലപ്രദമാണ് ചൂട് ചികിത്സഈ കേസിൽ ഉൽപ്പന്നങ്ങൾക്ക് എപ്പോഴത്തേതിനേക്കാൾ കൂടുതൽ സമയം ആവശ്യമാണ് സാധാരണ അവസ്ഥകൾ. ഏകദേശം 7000 മീറ്റർ ഉയരത്തിൽ, ജലത്തിൻ്റെ ചുട്ടുതിളക്കുന്ന പോയിൻ്റ് എത്തുന്നു, ഇത് അത്തരം സാഹചര്യങ്ങളിൽ പല ഉൽപ്പന്നങ്ങളും പാചകം ചെയ്യുന്നത് അസാധ്യമാക്കുന്നു.
തിളയ്ക്കുന്ന താപനില വസ്തുത ന് വിവിധ പദാർത്ഥങ്ങൾവ്യത്യസ്തമാണ്, പദാർത്ഥങ്ങളെ വേർതിരിക്കുന്നതിനുള്ള ചില സാങ്കേതികവിദ്യകൾ അടിസ്ഥാനമാക്കിയുള്ളതാണ്. ഉദാഹരണത്തിന്, നിരവധി ഘടകങ്ങൾ അടങ്ങിയ സങ്കീർണ്ണമായ ദ്രാവകമായ എണ്ണ ചൂടാക്കുന്നത് ഞങ്ങൾ പരിഗണിക്കുകയാണെങ്കിൽ, തിളപ്പിക്കുമ്പോൾ അതിനെ വ്യത്യസ്ത പദാർത്ഥങ്ങളായി തിരിക്കാം. IN ഈ സാഹചര്യത്തിൽ, മണ്ണെണ്ണ, ഗ്യാസോലിൻ, നാഫ്ത, ഇന്ധന എണ്ണ എന്നിവയുടെ തിളപ്പിക്കൽ പോയിൻ്റുകൾ വ്യത്യസ്തമാണെന്ന വസ്തുത കാരണം, വ്യത്യസ്ത ഊഷ്മാവിൽ ബാഷ്പീകരണത്തിലൂടെയും ഘനീഭവിക്കുന്നതിലൂടെയും പരസ്പരം വേർതിരിക്കാനാകും. ഈ പ്രക്രിയയെ സാധാരണയായി ഫ്രാക്ഷനേഷൻ (ചിത്രം 3) എന്ന് വിളിക്കുന്നു.

അരി. 3 എണ്ണയെ ഭിന്നസംഖ്യകളായി വേർതിരിക്കുക ()
ആരെയും പോലെ ശാരീരിക പ്രക്രിയ, തിളപ്പിക്കൽ ചില സംഖ്യാ മൂല്യം ഉപയോഗിച്ച് സ്വഭാവസവിശേഷതകളായിരിക്കണം, അത്തരമൊരു മൂല്യത്തെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം എന്ന് വിളിക്കുന്നു.
ഈ മൂല്യത്തിൻ്റെ ഭൗതിക അർത്ഥം മനസിലാക്കാൻ, ഇനിപ്പറയുന്ന ഉദാഹരണം പരിഗണിക്കുക: 1 കിലോ വെള്ളം എടുത്ത് തിളയ്ക്കുന്ന പോയിൻ്റിലേക്ക് കൊണ്ടുവരിക, തുടർന്ന് ഈ വെള്ളം പൂർണ്ണമായും ബാഷ്പീകരിക്കാൻ എത്ര ചൂട് ആവശ്യമാണെന്ന് അളക്കുക (താപനഷ്ടങ്ങൾ കണക്കിലെടുക്കാതെ) - ഈ മൂല്യം ജലത്തിൻ്റെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപത്തിന് തുല്യമായിരിക്കും. മറ്റൊരു പദാർത്ഥത്തിന്, ഈ താപ മൂല്യം വ്യത്യസ്തമായിരിക്കും, ഈ പദാർത്ഥത്തിൻ്റെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം ആയിരിക്കും.
ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക ചൂട് വളരെ മാറുന്നു പ്രധാന സ്വഭാവംആധുനിക ലോഹ നിർമ്മാണ സാങ്കേതികവിദ്യകളിൽ. ഉദാഹരണത്തിന്, ഇരുമ്പ് ഉരുകി ബാഷ്പീകരിക്കപ്പെടുമ്പോൾ, അതിൻ്റെ തുടർന്നുള്ള ഘനീഭവിച്ചും ഘനീഭവിക്കുമ്പോഴും, ക്രിസ്റ്റൽ സെൽയഥാർത്ഥ സാമ്പിളിനേക്കാൾ ഉയർന്ന ശക്തി നൽകുന്ന ഒരു ഘടനയോടെ.
പദവി: ബാഷ്പീകരണത്തിൻ്റെയും കാൻസൻസേഷൻ്റെയും പ്രത്യേക ചൂട് (ചിലപ്പോൾ സൂചിപ്പിച്ചിരിക്കുന്നു ).
യൂണിറ്റ്: .
ലബോറട്ടറി പരീക്ഷണങ്ങൾ ഉപയോഗിച്ച് പദാർത്ഥങ്ങളുടെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം നിർണ്ണയിക്കപ്പെടുന്നു, കൂടാതെ അടിസ്ഥാന പദാർത്ഥങ്ങൾക്കായുള്ള അതിൻ്റെ മൂല്യങ്ങൾ ഉചിതമായ പട്ടികയിൽ പട്ടികപ്പെടുത്തിയിരിക്കുന്നു.
|
പദാർത്ഥം |
ഒരു കെറ്റിലിലെ വെള്ളം 100˚C താപനിലയിൽ തിളച്ചുമറിയുന്നുവെന്ന് എല്ലാവർക്കും അറിയാം. എന്നാൽ തിളയ്ക്കുന്ന പ്രക്രിയയിൽ ജലത്തിൻ്റെ താപനില മാറുന്നില്ലെന്ന് നിങ്ങൾ ശ്രദ്ധിച്ചിട്ടുണ്ടോ? ചോദ്യം ഇതാണ് - നമ്മൾ നിരന്തരം കണ്ടെയ്നർ തീയിൽ സൂക്ഷിച്ചാൽ ഉൽപ്പാദിപ്പിക്കുന്ന ഊർജ്ജം എവിടെ പോകുന്നു? ഇത് ദ്രാവകത്തെ നീരാവിയാക്കി മാറ്റുന്നു. അങ്ങനെ, വെള്ളം ഒരു വാതകാവസ്ഥയിലേക്ക് രൂപാന്തരപ്പെടുത്തുന്നതിന്, താപത്തിൻ്റെ നിരന്തരമായ വിതരണം ആവശ്യമാണ്. ഒരു കിലോഗ്രാം ദ്രാവകത്തെ അതേ ഊഷ്മാവിൽ നീരാവി ആക്കി മാറ്റാൻ എത്രമാത്രം ആവശ്യമുണ്ട് എന്നത് ജലത്തിൻ്റെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം എന്ന് വിളിക്കപ്പെടുന്ന ഭൗതിക അളവ് നിർണ്ണയിക്കുന്നു.
അളവിൻ്റെ ഭൗതിക അർത്ഥം
തിളപ്പിക്കുന്നതിന് ഊർജ്ജം ആവശ്യമാണ്. ഇതിൽ ഭൂരിഭാഗവും ആറ്റങ്ങളും തന്മാത്രകളും തമ്മിലുള്ള രാസബന്ധങ്ങൾ തകർക്കാൻ ഉപയോഗിക്കുന്നു, അതിൻ്റെ ഫലമായി നീരാവി കുമിളകൾ രൂപം കൊള്ളുന്നു, കൂടാതെ ഒരു ചെറിയ ഭാഗം നീരാവി വികസിപ്പിക്കാൻ ഉപയോഗിക്കുന്നു, അതായത്, തത്ഫലമായുണ്ടാകുന്ന കുമിളകൾ പൊട്ടിച്ച് പുറത്തുവിടാൻ കഴിയും. ദ്രാവകം അതിൻ്റെ മുഴുവൻ ഊർജ്ജവും വാതകാവസ്ഥയിലേക്ക് മാറ്റുന്നതിനാൽ, അതിൻ്റെ "ബലങ്ങൾ" തീർന്നു. നിരന്തരം ഊർജ്ജം പുതുക്കുന്നതിനും തിളപ്പിക്കൽ നീട്ടുന്നതിനും, ദ്രാവകത്തോടുകൂടിയ കണ്ടെയ്നറിലേക്ക് കൂടുതൽ കൂടുതൽ ചൂട് നൽകണം. ഒരു ബോയിലറിന് അതിൻ്റെ വിതരണം നൽകാൻ കഴിയും, ഗ്യാസ് ബർണർഅല്ലെങ്കിൽ മറ്റേതെങ്കിലും ചൂടാക്കൽ ഉപകരണം. തിളപ്പിക്കുമ്പോൾ, ദ്രാവകത്തിൻ്റെ താപനില വർദ്ധിക്കുന്നില്ല; പ്രക്രിയ നടക്കുന്നുഒരേ താപനിലയിൽ നീരാവി രൂപീകരണം.
വ്യത്യസ്ത ദ്രാവകങ്ങൾ ആവശ്യമാണ് വ്യത്യസ്ത അളവുകൾനീരാവിയായി രൂപാന്തരപ്പെടാനുള്ള ചൂട്. ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം കാണിക്കുന്നത് ഏതാണ്.
ഒരു ഉദാഹരണത്തിൽ നിന്ന് ഈ മൂല്യം എങ്ങനെ നിർണ്ണയിക്കപ്പെടുന്നുവെന്ന് നിങ്ങൾക്ക് മനസ്സിലാക്കാം. 1 ലിറ്റർ വെള്ളം എടുത്ത് തിളപ്പിക്കുക. തുടർന്ന് എല്ലാ ദ്രാവകങ്ങളും ബാഷ്പീകരിക്കാൻ ആവശ്യമായ താപത്തിൻ്റെ അളവ് ഞങ്ങൾ അളക്കുന്നു, കൂടാതെ ജലത്തിനായി ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപത്തിൻ്റെ മൂല്യം നേടുകയും ചെയ്യുന്നു. മറ്റുള്ളവർക്ക് രാസ സംയുക്തങ്ങൾഈ കണക്ക് വ്യത്യസ്തമായിരിക്കും.
ഭൗതികശാസ്ത്രത്തിൽ, ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപത്തെ സൂചിപ്പിക്കുന്നു ലാറ്റിൻ അക്ഷരം L. ഇത് ഒരു കിലോഗ്രാം ജൂൾസിൽ (J/kg) അളക്കുന്നു. ബാഷ്പീകരണത്തിനായി ചെലവഴിക്കുന്ന താപത്തെ ദ്രാവകത്തിൻ്റെ പിണ്ഡം കൊണ്ട് ഹരിച്ചാൽ ഇത് ലഭിക്കും:
ഈ മൂല്യം വളരെ പ്രധാനമാണ് ഉത്പാദന പ്രക്രിയകൾഅടിസ്ഥാനമാക്കിയുള്ളത് ആധുനിക സാങ്കേതികവിദ്യകൾ. ഉദാഹരണത്തിന്, ലോഹങ്ങളുടെ ഉത്പാദനത്തിൽ അവർ അതിൽ ശ്രദ്ധ കേന്ദ്രീകരിക്കുന്നു. ഇരുമ്പ് ഉരുകുകയും പിന്നീട് ഘനീഭവിക്കുകയും ചെയ്താൽ, കൂടുതൽ കഠിനമാക്കുമ്പോൾ ശക്തമായ ഒരു ക്രിസ്റ്റൽ ലാറ്റിസ് രൂപം കൊള്ളുന്നു.
ഇത് എന്തിന് തുല്യമാണ്
വിവിധ പദാർത്ഥങ്ങളുടെ പ്രത്യേക താപ മൂല്യം (r) ലബോറട്ടറി പഠനങ്ങളിൽ നിർണ്ണയിക്കപ്പെട്ടു. സാധാരണ അന്തരീക്ഷമർദ്ദത്തിലുള്ള ജലം 100 ഡിഗ്രി സെൽഷ്യസിൽ തിളച്ചുമറിയുന്നു, ജലത്തിൻ്റെ ബാഷ്പീകരണത്തിൻ്റെ താപം 2258.2 kJ/kg ആണ്. മറ്റ് ചില പദാർത്ഥങ്ങളുടെ ഈ സൂചകം പട്ടികയിൽ നൽകിയിരിക്കുന്നു:
| പദാർത്ഥം | തിളയ്ക്കുന്ന സ്ഥലം, °C | r, kJ/kg |
|---|---|---|
| നൈട്രജൻ | -196 | 198 |
| ഹീലിയം | -268,94 | 20,6 |
| ഹൈഡ്രജൻ | -253 | 454 |
| ഓക്സിജൻ | -183 | 213 |
| കാർബൺ | 4350 | 50000 |
| ഫോസ്ഫറസ് | 280 | 400 |
| മീഥെയ്ൻ | -162 | 510 |
| പെൻ്റെയ്ൻ | 36 | 360 |
| ഇരുമ്പ് | 2735 | 6340 |
| ചെമ്പ് | 2590 | 4790 |
| ടിൻ | 2430 | 2450 |
| നയിക്കുക | 1750 | 8600 |
| സിങ്ക് | 907 | 1755 |
| മെർക്കുറി | 357 | 285 |
| സ്വർണ്ണം | 2 700 | 1 650 |
| എത്തനോൾ | 78 | 840 |
| മീഥൈൽ ആൽക്കഹോൾ | 65 | 1100 |
| ക്ലോറോഫോം | 61 | 279 |
എന്നിരുന്നാലും, ചില ഘടകങ്ങളുടെ സ്വാധീനത്തിൽ ഈ സൂചകം മാറിയേക്കാം:
- താപനില.ഇത് വർദ്ധിക്കുന്നതിനനുസരിച്ച്, ബാഷ്പീകരണത്തിൻ്റെ ചൂട് കുറയുകയും പൂജ്യത്തിന് തുല്യമാകുകയും ചെയ്യും.
t, °C r, kJ/kg 2500 10 2477 20 2453 50 2380 80 2308 100 2258 200 1940 300 1405 374 115 374,15 - സമ്മർദ്ദം.മർദ്ദം കുറയുമ്പോൾ, ബാഷ്പീകരണത്തിൻ്റെ ചൂട് വർദ്ധിക്കുന്നു, തിരിച്ചും. തിളയ്ക്കുന്ന പോയിൻ്റ് മർദ്ദത്തിന് നേരിട്ട് ആനുപാതികമാണ്, കൂടാതെ 374 ° C എന്ന നിർണായക മൂല്യത്തിൽ എത്താൻ കഴിയും.
പി, പാ ടി തിളപ്പിക്കുക., °C r, kJ/kg 0,0123 10 2477 0,1234 50 2380 1 100 2258 2 120 2202 5 152 2014 10 180 1889 20 112 1638 50 264 1638 100 311 1316 200 366 585 220 373,7 184,8 ഗുരുതരം 221.29 374,15 - - പദാർത്ഥത്തിൻ്റെ പിണ്ഡം.പ്രക്രിയയിൽ ഉൾപ്പെടുന്ന താപത്തിൻ്റെ അളവ് രൂപംകൊണ്ട നീരാവി പിണ്ഡത്തിന് നേരിട്ട് ആനുപാതികമാണ്.
ബാഷ്പീകരണവും ഘനീഭവിക്കുന്നതും തമ്മിലുള്ള ബന്ധം
ബാഷ്പീകരണത്തിന് വിപരീതമായ പ്രക്രിയ - ഘനീഭവിക്കൽ - നീരാവി അതിൻ്റെ രൂപീകരണത്തിന് ഉപയോഗിച്ച അതേ ഊർജ്ജം ചെലവഴിക്കുന്നതായി ഭൗതികശാസ്ത്രജ്ഞർ കണ്ടെത്തി. ഈ നിരീക്ഷണം ഊർജ്ജ സംരക്ഷണ നിയമം സ്ഥിരീകരിക്കുന്നു.
അല്ലെങ്കിൽ, ദ്രാവകം ബാഷ്പീകരിക്കപ്പെടുകയും പിന്നീട് ഘനീഭവിക്കുകയും ചെയ്യുന്ന ഒരു ഇൻസ്റ്റാളേഷൻ സൃഷ്ടിക്കാൻ കഴിയും. ബാഷ്പീകരണത്തിന് ആവശ്യമായ താപവും ഘനീഭവിക്കുന്നതിന് ആവശ്യമായ താപവും തമ്മിലുള്ള വ്യത്യാസം മറ്റ് ആവശ്യങ്ങൾക്ക് ഉപയോഗിക്കാവുന്ന ഊർജ്ജത്തിൻ്റെ സംഭരണത്തിന് കാരണമാകും. സാരാംശത്തിൽ, ഒരു ശാശ്വത ചലന യന്ത്രം സൃഷ്ടിക്കപ്പെടും. എന്നാൽ ഇത് ഭൗതിക നിയമങ്ങൾക്ക് വിരുദ്ധമാണ്, അതായത് അത് അസാധ്യമാണ്.
അത് എങ്ങനെയാണ് അളക്കുന്നത്?
- ജലത്തിൻ്റെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം ഫിസിക്കൽ ലബോറട്ടറികളിൽ പരീക്ഷണാത്മകമായി അളക്കുന്നു. ഇതിനായി കലോറിമീറ്ററുകൾ ഉപയോഗിക്കുന്നു. നടപടിക്രമം ഇതുപോലെ കാണപ്പെടുന്നു:
- ഒരു നിശ്ചിത അളവിലുള്ള ദ്രാവകം കലോറിമീറ്ററിലേക്ക് ഒഴിക്കുന്നു.
ദ്രവ്യത്തെ മാറ്റുന്ന പ്രതിഭാസം ദ്രാവകാവസ്ഥവാതകത്തിലേക്ക് വിളിക്കുന്നു ബാഷ്പീകരണം. ബാഷ്പീകരണം രണ്ട് പ്രക്രിയകളുടെ രൂപത്തിൽ നടത്താം: i.
തിളച്ചുമറിയുന്നു
ബാഷ്പീകരണത്തിൻ്റെ രണ്ടാമത്തെ പ്രക്രിയ തിളപ്പിക്കലാണ്. ഒരു ഗ്ലാസ് ഫ്ലാസ്കിൽ വെള്ളം ചൂടാക്കി ലളിതമായ ഒരു പരീക്ഷണം ഉപയോഗിച്ച് ഈ പ്രക്രിയ നിരീക്ഷിക്കാവുന്നതാണ്. വെള്ളം ചൂടാക്കുമ്പോൾ, കുറച്ച് സമയത്തിന് ശേഷം അതിൽ കുമിളകൾ പ്രത്യക്ഷപ്പെടുന്നു, അതിൽ വായുവും പൂരിത ജല നീരാവിയും അടങ്ങിയിരിക്കുന്നു, ഇത് കുമിളകൾക്കുള്ളിൽ വെള്ളം ബാഷ്പീകരിക്കപ്പെടുമ്പോൾ രൂപം കൊള്ളുന്നു. ഊഷ്മാവ് ഉയരുമ്പോൾ, കുമിളകൾക്കുള്ളിലെ മർദ്ദം വർദ്ധിക്കുകയും, ബൂയൻ്റ് ഫോഴ്സിൻ്റെ സ്വാധീനത്തിൽ അവ മുകളിലേക്ക് ഉയരുകയും ചെയ്യുന്നു. എന്നിരുന്നാലും, ജലത്തിൻ്റെ മുകളിലെ പാളികളുടെ താപനില താഴ്ന്നതിനേക്കാൾ കുറവായതിനാൽ, കുമിളകളിലെ നീരാവി ഘനീഭവിക്കാൻ തുടങ്ങുകയും അവ ചുരുങ്ങുകയും ചെയ്യുന്നു. മുഴുവൻ അളവിലും വെള്ളം ചൂടാകുമ്പോൾ, നീരാവി ഉള്ള കുമിളകൾ ഉപരിതലത്തിലേക്ക് ഉയരുകയും പൊട്ടിത്തെറിക്കുകയും നീരാവി പുറത്തുവരുകയും ചെയ്യുന്നു. വെള്ളം തിളച്ചുമറിയുകയാണ്. കുമിളകളിലെ പൂരിത നീരാവി മർദ്ദം അന്തരീക്ഷമർദ്ദത്തിന് തുല്യമായ താപനിലയിലാണ് ഇത് സംഭവിക്കുന്നത്.
ഒരു നിശ്ചിത താപനിലയിൽ ദ്രാവകത്തിൻ്റെ മുഴുവൻ അളവിലും സംഭവിക്കുന്ന ബാഷ്പീകരണ പ്രക്രിയയെ വിളിക്കുന്നു. ഒരു ദ്രാവകം തിളയ്ക്കുന്ന താപനിലയെ വിളിക്കുന്നു തിളനില.
ഈ താപനില അന്തരീക്ഷമർദ്ദത്തെ ആശ്രയിച്ചിരിക്കുന്നു. അന്തരീക്ഷമർദ്ദം കൂടുന്നതിനനുസരിച്ച് തിളയ്ക്കുന്ന പോയിൻ്റ് വർദ്ധിക്കുന്നു.
ചുട്ടുതിളക്കുന്ന പ്രക്രിയയിൽ, ദ്രാവകത്തിൻ്റെ താപനില മാറില്ല, ഊർജ്ജം പുറത്തുനിന്നാണ് വരുന്നത് എന്ന വസ്തുത ഉണ്ടായിരുന്നിട്ടും അനുഭവം കാണിക്കുന്നു. തിളയ്ക്കുന്ന പോയിൻ്റിൽ ഒരു ദ്രാവകം വാതകാവസ്ഥയിലേക്ക് മാറുന്നത് തന്മാത്രകൾ തമ്മിലുള്ള ദൂരത്തിൻ്റെ വർദ്ധനവുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു, അതനുസരിച്ച് അവയ്ക്കിടയിലുള്ള ആകർഷണത്തെ മറികടക്കുന്നു. ദ്രാവകത്തിലേക്ക് വിതരണം ചെയ്യുന്ന ഊർജ്ജം ആകർഷണ ശക്തികളെ മറികടക്കാൻ പ്രവർത്തിക്കാൻ ഉപയോഗിക്കുന്നു. എല്ലാ ദ്രാവകവും നീരാവിയായി മാറുന്നതുവരെ ഇത് സംഭവിക്കുന്നു. തിളപ്പിക്കുമ്പോൾ ദ്രാവകവും നീരാവിയും ഒരേ താപനിലയുള്ളതിനാൽ, ശരാശരി ഗതികോർജ്ജംതന്മാത്രകൾ മാറുന്നില്ല, അവയുടെ സാധ്യതയുള്ള ഊർജ്ജം വർദ്ധിക്കുന്നു.
റൂം താപനിലയിൽ നിന്ന് തിളയ്ക്കുന്ന പോയിൻ്റ് (എബി), തിളപ്പിക്കൽ പോയിൻ്റ് (ബിസി), നീരാവി ചൂടാക്കൽ (സിഡി), സ്റ്റീം കൂളിംഗ് (ഡിഇ), കണ്ടൻസേഷൻ (ഇഎഫ്), തുടർന്നുള്ള തണുപ്പിക്കൽ എന്നിവയ്ക്കിടയിലുള്ള ജലത്തിൻ്റെ താപനിലയുടെ ഗ്രാഫ് ചിത്രം കാണിക്കുന്നു. (FG) .
ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക ചൂട്
ഒരു ദ്രാവകത്തിൽ നിന്ന് വാതകാവസ്ഥയിലേക്ക് വ്യത്യസ്ത പദാർത്ഥങ്ങളെ രൂപാന്തരപ്പെടുത്തുന്നതിന്, വ്യത്യസ്ത ഊർജ്ജം ആവശ്യമാണ്, ഈ ഊർജ്ജത്തെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം എന്ന് വിളിക്കുന്ന ഒരു മൂല്യമാണ്.
ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക ചൂട് (എൽ) 1 കി.ഗ്രാം ഭാരമുള്ള ഒരു വസ്തുവിനെ തിളയ്ക്കുന്ന ഘട്ടത്തിൽ ദ്രാവകാവസ്ഥയിൽ നിന്ന് വാതകാവസ്ഥയിലേക്ക് മാറ്റാൻ നൽകേണ്ട താപത്തിൻ്റെ അളവിൻ്റെ അനുപാതത്തിന് തുല്യമായ മൂല്യമാണ്.
ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപത്തിൻ്റെ യൂണിറ്റ് - [ എൽ] = J/kg.
ഒരു ദ്രാവകത്തിൽ നിന്ന് വാതകാവസ്ഥയിലേക്ക് മാറുന്നതിന് mn പിണ്ഡമുള്ള ഒരു പദാർത്ഥത്തിന് നൽകേണ്ട താപത്തിൻ്റെ അളവ് കണക്കാക്കാൻ, ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം ( എൽപദാർത്ഥത്തിൻ്റെ പിണ്ഡം കൊണ്ട് ഗുണിച്ചാൽ: Q = Lm.
നീരാവി ഘനീഭവിക്കുമ്പോൾ, ഒരു നിശ്ചിത അളവിലുള്ള താപം പുറത്തുവരുന്നു, അതിൻ്റെ മൂല്യം ഒരേ താപനിലയിൽ ദ്രാവകത്തെ നീരാവിയായി മാറ്റാൻ ചെലവഴിക്കേണ്ട താപത്തിൻ്റെ അളവിന് തുല്യമാണ്.
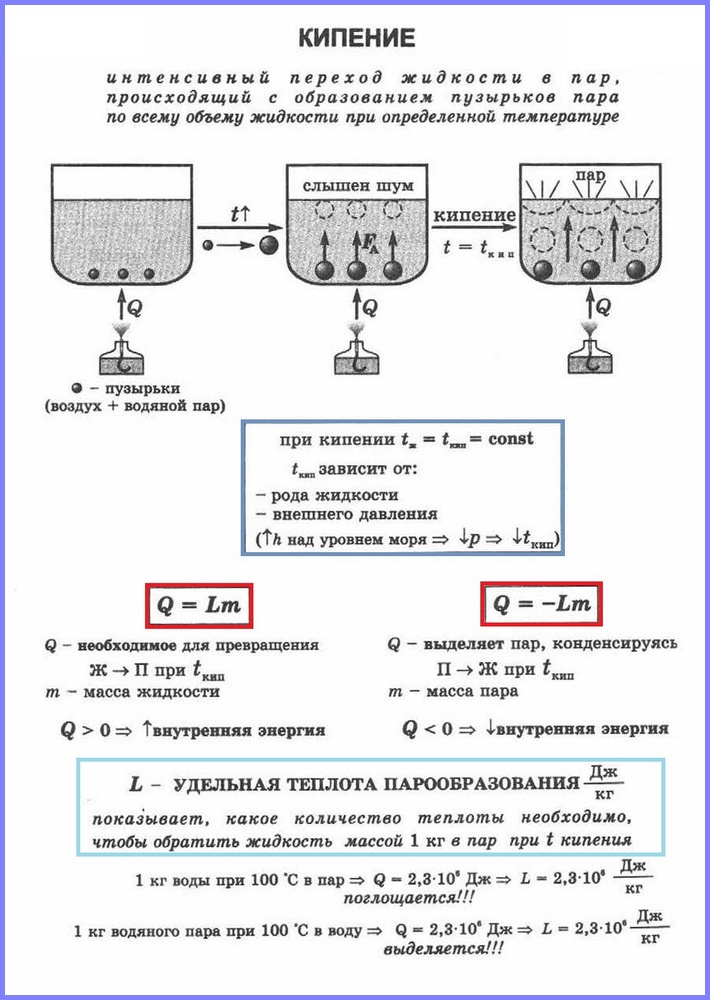
ഒരു ദ്രാവകം ഉപരിതലത്തിൽ നിന്ന് മാത്രമല്ല, അതിനകത്തും ചൂടാക്കുമ്പോൾ ഉണ്ടാകുന്ന തീവ്രമായ ബാഷ്പീകരണമാണ് തിളപ്പിക്കൽ.
താപം ആഗിരണം ചെയ്യുന്നതിലൂടെ തിളപ്പിക്കൽ സംഭവിക്കുന്നു.
വിതരണം ചെയ്ത താപത്തിൻ്റെ ഭൂരിഭാഗവും പദാർത്ഥത്തിൻ്റെ കണികകൾ തമ്മിലുള്ള ബന്ധങ്ങൾ തകർക്കുന്നതിനാണ് ചെലവഴിക്കുന്നത്, ബാക്കിയുള്ളത് - നീരാവി വിപുലീകരണ സമയത്ത് ചെയ്യുന്ന ജോലികൾക്കായി.
തൽഫലമായി, നീരാവി കണികകൾ തമ്മിലുള്ള പ്രതിപ്രവർത്തന ഊർജ്ജം ദ്രാവക കണികകൾക്കിടയിലുള്ളതിനേക്കാൾ വലുതായിത്തീരുന്നു, അതിനാൽ നീരാവിയുടെ ആന്തരിക ഊർജ്ജം ഒരേ താപനിലയിൽ ദ്രാവകത്തിൻ്റെ ആന്തരിക ഊർജ്ജത്തേക്കാൾ വലുതാണ്.
തിളയ്ക്കുന്ന പ്രക്രിയയിൽ ദ്രാവകത്തെ നീരാവിയാക്കി മാറ്റാൻ ആവശ്യമായ താപത്തിൻ്റെ അളവ് ഫോർമുല ഉപയോഗിച്ച് കണക്കാക്കാം:

ഇവിടെ m എന്നത് ദ്രാവകത്തിൻ്റെ പിണ്ഡം (കിലോ) ആണ്
ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപമാണ് എൽ.
ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം തിളയ്ക്കുന്ന പോയിൻ്റിൽ തന്നിരിക്കുന്ന ഒരു പദാർത്ഥത്തിൻ്റെ 1 കി.ഗ്രാം ആവിയായി മാറ്റാൻ എത്ര ചൂട് ആവശ്യമാണെന്ന് കാണിക്കുന്നു. SI സിസ്റ്റത്തിലെ ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപത്തിൻ്റെ യൂണിറ്റ്:
[L] = 1 J/kg
വർദ്ധിച്ചുവരുന്ന മർദ്ദം കൊണ്ട്, ദ്രാവകത്തിൻ്റെ തിളപ്പിക്കൽ പോയിൻ്റ് വർദ്ധിക്കുന്നു, ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക ചൂട് കുറയുന്നു, തിരിച്ചും.

തിളപ്പിക്കുമ്പോൾ, ദ്രാവകത്തിൻ്റെ താപനില മാറില്ല.
തിളയ്ക്കുന്ന സ്ഥലം ദ്രാവകത്തിൽ ചെലുത്തുന്ന സമ്മർദ്ദത്തെ ആശ്രയിച്ചിരിക്കുന്നു.
ഒരേ മർദ്ദത്തിലുള്ള ഓരോ പദാർത്ഥത്തിനും അതിൻ്റേതായ തിളപ്പിക്കൽ പോയിൻ്റുണ്ട്.
അന്തരീക്ഷമർദ്ദം വർദ്ധിക്കുന്നതിനനുസരിച്ച്, തിളപ്പിക്കൽ ഉയർന്ന താപനിലയിൽ ആരംഭിക്കുന്നു, മർദ്ദം കുറയുമ്പോൾ, തിരിച്ചും.
ഉദാഹരണത്തിന്, സാധാരണ അന്തരീക്ഷമർദ്ദത്തിൽ മാത്രം വെള്ളം 100 ഡിഗ്രി സെൽഷ്യസിൽ തിളച്ചുമറിയുന്നു.
തിളപ്പിക്കുമ്പോൾ ഒരു ദ്രാവകത്തിനുള്ളിൽ എന്താണ് സംഭവിക്കുന്നത്?

ദ്രാവകത്തിൽ നീരാവി കുമിളകളുടെ തുടർച്ചയായ രൂപീകരണവും വളർച്ചയും ഉള്ള ഒരു ദ്രാവകം നീരാവിയായി മാറുന്നതാണ് തിളപ്പിക്കൽ. ചൂടാക്കലിൻ്റെ തുടക്കത്തിൽ, വെള്ളം വായുവിൽ പൂരിതമാവുകയും ഊഷ്മാവിൽ ആയിരിക്കും. വെള്ളം ചൂടാക്കുമ്പോൾ, അതിൽ അലിഞ്ഞുചേർന്ന വാതകം പാത്രത്തിൻ്റെ അടിയിലും ചുവരുകളിലും പുറത്തുവിടുകയും വായു കുമിളകൾ ഉണ്ടാക്കുകയും ചെയ്യുന്നു. തിളയ്ക്കുന്നതിന് വളരെ മുമ്പുതന്നെ അവ പ്രത്യക്ഷപ്പെടാൻ തുടങ്ങുന്നു. ഈ കുമിളകളിലേക്ക് വെള്ളം ബാഷ്പീകരിക്കപ്പെടുന്നു. നീരാവി നിറച്ച ഒരു കുമിള ആവശ്യത്തിന് ഉയർന്ന താപനിലയിൽ വീർക്കാൻ തുടങ്ങുന്നു.

ഒരു നിശ്ചിത വലുപ്പത്തിൽ എത്തിയ ശേഷം, അത് അടിയിൽ നിന്ന് പൊട്ടി, ജലത്തിൻ്റെ ഉപരിതലത്തിലേക്ക് ഉയർന്ന് പൊട്ടിത്തെറിക്കുന്നു. ഈ സാഹചര്യത്തിൽ, നീരാവി ദ്രാവകം ഉപേക്ഷിക്കുന്നു. വെള്ളം വേണ്ടത്ര ചൂടാക്കിയില്ലെങ്കിൽ, തണുത്ത പാളികളിലേക്ക് ഉയരുന്ന നീരാവി കുമിള തകരുന്നു. തത്ഫലമായുണ്ടാകുന്ന ജലത്തിലെ ഏറ്റക്കുറച്ചിലുകൾ ജലത്തിൻ്റെ മുഴുവൻ അളവിലും ധാരാളം ചെറിയ വായു കുമിളകൾ പ്രത്യക്ഷപ്പെടുന്നതിലേക്ക് നയിക്കുന്നു: "വൈറ്റ് കീ" എന്ന് വിളിക്കപ്പെടുന്നവ.

പാത്രത്തിൻ്റെ അടിയിൽ ഒരു വോളിയം ഉള്ള ഒരു എയർ ബബിൾ ബാധിക്കുന്നു ഉയർത്തുക:
ഫണ്ടർ = ഫാർക്കിമിഡിസ് - എഫ്ഗ്രാവിറ്റി
ബബിൾ അടിയിലേക്ക് അമർത്തിയാൽ കാരണം താഴെയുള്ള ഉപരിതലംസമ്മർദ്ദ ശക്തികൾ പ്രവർത്തിക്കുന്നില്ല. ചൂടാക്കുമ്പോൾ, വാതകം പുറത്തുവിടുന്നത് കാരണം കുമിള വികസിക്കുകയും ലിഫ്റ്റിംഗ് ഫോഴ്സ് അമർത്തുന്ന ശക്തിയേക്കാൾ അല്പം കൂടുതലായിരിക്കുമ്പോൾ അടിയിൽ നിന്ന് പൊട്ടുകയും ചെയ്യുന്നു. താഴെ നിന്ന് പൊട്ടാൻ കഴിയുന്ന കുമിളയുടെ വലിപ്പം അതിൻ്റെ ആകൃതിയെ ആശ്രയിച്ചിരിക്കുന്നു. താഴെയുള്ള കുമിളകളുടെ ആകൃതി നിർണ്ണയിക്കുന്നത് പാത്രത്തിൻ്റെ അടിഭാഗത്തെ നനവാണ്.
താഴെയുള്ള കുമിളകൾ നനയ്ക്കുന്നതിൻ്റെയും ലയിക്കുന്നതിൻ്റെയും അസന്തുലിതാവസ്ഥ അവയുടെ വലുപ്പം വർദ്ധിപ്പിക്കുന്നതിന് കാരണമായി. ചെയ്തത് വലിയ വലിപ്പങ്ങൾകുമിള ഉയരുമ്പോൾ, അതിന് പിന്നിൽ ശൂന്യതകളും വിള്ളലുകളും പ്രക്ഷുബ്ധതകളും രൂപം കൊള്ളുന്നു.
ഒരു കുമിള പൊട്ടുമ്പോൾ, അതിനെ ചുറ്റിപ്പറ്റിയുള്ള എല്ലാ ദ്രാവകവും കുതിച്ചുചാടി, ഒരു റിംഗ് വേവ് സൃഷ്ടിക്കുന്നു. അടയ്ക്കുമ്പോൾ, അത് ജലത്തിൻ്റെ ഒരു നിര എറിയുന്നു.

പൊട്ടിത്തെറിക്കുന്ന കുമിളകൾ തകരുമ്പോൾ, അൾട്രാസോണിക് ആവൃത്തികളുടെ ഷോക്ക് തരംഗങ്ങൾ ദ്രാവകത്തിൽ പ്രചരിക്കുന്നു, ഒപ്പം കേൾക്കാവുന്ന ശബ്ദവും. തിളപ്പിക്കുന്നതിൻ്റെ പ്രാരംഭ ഘട്ടങ്ങൾ ഏറ്റവും ഉച്ചത്തിലുള്ളതും ഉയർന്നതുമായ ശബ്ദങ്ങളാൽ സവിശേഷതയാണ് ("ഘട്ടത്തിൽ" വെളുത്ത കീ"ചായക്കട്ടി പാടുന്നു").
(ഉറവിടം: virlib.eunnet.net)
ജലസംസ്ഥാനങ്ങളിലെ മാറ്റങ്ങളുടെ താപനില ഷെഡ്യൂൾ

ബുക്ക്ഷെൽഫിലേക്ക് നോക്കൂ!
താൽപ്പര്യമുള്ളത്
എന്തിനാണ് അവർ ടീപ്പോയുടെ അടപ്പിൽ ഒരു ദ്വാരം ഉണ്ടാക്കുന്നത്?
നീരാവി പുറത്തുവിടാൻ. ലിഡിൽ ദ്വാരമില്ലാതെ, നീരാവി കെറ്റിൽ സ്പൗട്ടിൽ നിന്ന് വെള്ളം തെറിപ്പിക്കും.
___
പാകം ചെയ്യുന്ന ഉരുളക്കിഴങ്ങ് സമയദൈർഘ്യം, തിളയ്ക്കുന്ന നിമിഷം മുതൽ, ഹീറ്ററിൻ്റെ ശക്തിയെ ആശ്രയിക്കുന്നില്ല. ഉൽപന്നം തിളയ്ക്കുന്ന ഘട്ടത്തിൽ നിലനിൽക്കുന്ന സമയമാണ് ദൈർഘ്യം നിർണ്ണയിക്കുന്നത്.
ഹീറ്ററിൻ്റെ ശക്തി തിളയ്ക്കുന്ന പോയിൻ്റിനെ ബാധിക്കില്ല, പക്ഷേ ജലത്തിൻ്റെ ബാഷ്പീകരണ നിരക്ക് മാത്രമേ ബാധിക്കുകയുള്ളൂ.
തിളപ്പിക്കുന്നത് വെള്ളം മരവിപ്പിക്കാൻ ഇടയാക്കും. ഇത് ചെയ്യുന്നതിന്, വെള്ളം സ്ഥിതിചെയ്യുന്ന പാത്രത്തിൽ നിന്ന് വായുവും നീരാവിയും പമ്പ് ചെയ്യേണ്ടത് ആവശ്യമാണ്, അങ്ങനെ വെള്ളം എല്ലാ സമയത്തും തിളച്ചുമറിയുന്നു.
“ചട്ടികൾ അരികിൽ എളുപ്പത്തിൽ തിളപ്പിക്കുന്നു - മോശം കാലാവസ്ഥ!”
മോശം കാലാവസ്ഥയ്ക്കൊപ്പം അന്തരീക്ഷമർദ്ദം കുറയുന്നതാണ് പാൽ വേഗത്തിൽ ഓടിപ്പോകാനുള്ള കാരണം.
___
ആഴത്തിലുള്ള ഖനികളുടെ അടിയിൽ വളരെ ചൂടുള്ള ചുട്ടുതിളക്കുന്ന വെള്ളം ലഭിക്കും, അവിടെ വായു മർദ്ദം ഭൂമിയുടെ ഉപരിതലത്തേക്കാൾ വളരെ കൂടുതലാണ്. അതിനാൽ 300 മീറ്റർ താഴ്ചയിൽ, വെള്ളം 101 × C ൽ തിളയ്ക്കും.
എയർ പമ്പിൻ്റെ മണിയുടെ കീഴിൽ നിങ്ങൾക്ക് 20 × സിയിൽ "തിളക്കുന്ന വെള്ളം" ലഭിക്കും.
ചൊവ്വയിൽ നമ്മൾ 45 സെൽഷ്യസിൽ "തിളച്ച വെള്ളം" കുടിക്കും.
ഉപ്പുവെള്ളം 100 സിക്ക് മുകളിലുള്ള താപനിലയിൽ തിളപ്പിക്കുന്നു. ___
പർവതപ്രദേശങ്ങളിൽ ഗണ്യമായ ഉയരത്തിലും താഴ്ന്ന അന്തരീക്ഷമർദ്ദത്തിലും, 100 സെൽഷ്യസിൽ താഴെയുള്ള താപനിലയിൽ വെള്ളം തിളച്ചുമറിയുന്നു.

അത്തരമൊരു ഭക്ഷണം പാകം ചെയ്യുന്നതിനായി കാത്തിരിക്കാൻ കൂടുതൽ സമയമെടുക്കും.
കുറച്ച് തണുത്ത വെള്ളം ഒഴിക്കുക ... അത് തിളയ്ക്കും!
സാധാരണ വെള്ളം 100 ഡിഗ്രി സെൽഷ്യസിലാണ് തിളയ്ക്കുന്നത്. ഫ്ലാസ്കിലെ വെള്ളം തിളയ്ക്കുന്നത് വരെ ബർണറിൽ ചൂടാക്കുക. നമുക്ക് ബർണർ ഓഫ് ചെയ്യാം. വെള്ളം തിളയ്ക്കുന്നത് നിർത്തുന്നു. ഒരു സ്റ്റോപ്പർ ഉപയോഗിച്ച് ഫ്ലാസ്ക് അടച്ച് ഒരു സ്ട്രീമിലെ സ്റ്റോപ്പറിലേക്ക് ശ്രദ്ധാപൂർവ്വം തണുത്ത വെള്ളം ഒഴിക്കാൻ തുടങ്ങുക. അത് എങ്ങനെയുള്ളതാണ്? വെള്ളം വീണ്ടും തിളച്ചുമറിയുന്നു!
..............................സ്ട്രീമിന് താഴെ തണുത്ത വെള്ളംഫ്ലാസ്കിലെ വെള്ളം, അതോടൊപ്പം നീരാവി തണുക്കാൻ തുടങ്ങുന്നു.
നീരാവിയുടെ അളവ് കുറയുകയും ജലത്തിൻ്റെ ഉപരിതലത്തിന് മുകളിലുള്ള മർദ്ദം മാറുകയും ചെയ്യുന്നു ...
ഏത് ദിശയിലാണ് നിങ്ങൾ ചിന്തിക്കുന്നത്?
... കുറഞ്ഞ മർദ്ദത്തിൽ വെള്ളത്തിൻ്റെ തിളയ്ക്കുന്ന പോയിൻ്റ് 100 ഡിഗ്രിയിൽ താഴെയാണ്, ഫ്ലാസ്കിലെ വെള്ളം വീണ്ടും തിളച്ചുമറിയുന്നു!
____
പാചകം ചെയ്യുമ്പോൾ, പാൻ ഉള്ളിലെ മർദ്ദം - "പ്രഷർ കുക്കർ" - ഏകദേശം 200 kPa ആണ്, അത്തരമൊരു ചട്ടിയിൽ സൂപ്പ് വളരെ വേഗത്തിൽ പാകം ചെയ്യും.
നിങ്ങൾക്ക് സിറിഞ്ചിൽ പകുതിയോളം വെള്ളം നിറയ്ക്കാനും അതേ സ്റ്റോപ്പർ ഉപയോഗിച്ച് അടച്ച് പ്ലങ്കർ കുത്തനെ വലിക്കാനും കഴിയും. വെള്ളത്തിൽ കുമിളകളുടെ ഒരു പിണ്ഡം പ്രത്യക്ഷപ്പെടും, ഇത് തിളയ്ക്കുന്ന വെള്ളത്തിൻ്റെ പ്രക്രിയ ആരംഭിച്ചുവെന്ന് സൂചിപ്പിക്കുന്നു (ഇത് ഊഷ്മാവിലാണ്!).
___
ഒരു പദാർത്ഥം വാതകാവസ്ഥയിലേക്ക് കടക്കുമ്പോൾ, അതിൻ്റെ സാന്ദ്രത ഏകദേശം 1000 മടങ്ങ് കുറയുന്നു.
___
ആദ്യത്തെ ഇലക്ട്രിക് കെറ്റിലുകൾക്ക് അടിയിൽ ഹീറ്ററുകൾ ഉണ്ടായിരുന്നു. വെള്ളം ഹീറ്ററുമായി സമ്പർക്കം പുലർത്തുന്നില്ല, തിളപ്പിക്കാൻ വളരെ സമയമെടുത്തു. 1923-ൽ ആർതർ ലാർജ് ഒരു കണ്ടുപിടുത്തം നടത്തി: അദ്ദേഹം ഒരു ഹീറ്റർ ഒരു പ്രത്യേക സ്ഥലത്ത് സ്ഥാപിച്ചു ചെമ്പ് ട്യൂബ്ടീപ്പോയ്ക്കുള്ളിൽ വെച്ചു. വെള്ളം പെട്ടെന്ന് തിളച്ചു കൊണ്ടിരുന്നു.
ശീതളപാനീയങ്ങൾക്കായി സ്വയം തണുപ്പിക്കുന്ന ക്യാനുകൾ യുഎസ്എയിൽ വികസിപ്പിച്ചെടുത്തിട്ടുണ്ട്. തുരുത്തിയിൽ കുറഞ്ഞ തിളയ്ക്കുന്ന ദ്രാവകമുള്ള ഒരു അറയുണ്ട്. ഒരു ചൂടുള്ള ദിവസത്തിൽ നിങ്ങൾ കാപ്സ്യൂൾ ചതച്ചാൽ, ദ്രാവകം വേഗത്തിൽ തിളപ്പിക്കാൻ തുടങ്ങും, പാത്രത്തിലെ ഉള്ളടക്കത്തിൽ നിന്ന് ചൂട് എടുക്കും, 90 സെക്കൻഡിനുള്ളിൽ പാനീയത്തിൻ്റെ താപനില 20-25 ഡിഗ്രി സെൽഷ്യസ് കുറയുന്നു.
ശരി, എന്തുകൊണ്ട് അങ്ങനെ?
നിങ്ങൾ എന്താണ് ചിന്തിക്കുന്നത്, 100 ഡിഗ്രി സെൽഷ്യസിൽ താഴെയുള്ള താപനിലയിൽ വെള്ളം തിളച്ചാൽ മുട്ട കഠിനമായി വേവിക്കാൻ കഴിയുമോ?
____
തിളയ്ക്കുന്ന മറ്റൊരു പാത്രത്തിൽ പൊങ്ങിക്കിടക്കുന്ന ഒരു പാത്രത്തിൽ വെള്ളം തിളപ്പിക്കുമോ?
എന്തുകൊണ്ട്? ___
വെള്ളം ചൂടാക്കാതെ തിളപ്പിക്കാമോ?

ഈ അറിവ് പെട്ടെന്ന് അപ്രത്യക്ഷമാകുന്നു, ക്രമേണ ആളുകൾ പരിചിതമായ പ്രതിഭാസങ്ങളുടെ സാരാംശം ശ്രദ്ധിക്കുന്നത് നിർത്തുന്നു. ചിലപ്പോൾ സൈദ്ധാന്തിക അറിവ് ഓർമ്മിക്കുന്നത് ഉപയോഗപ്രദമാണ്.
നിർവ്വചനം
തിളയ്ക്കുന്നത് എന്താണ്? ദ്രാവകത്തിൻ്റെ സ്വതന്ത്രമായ ഉപരിതലത്തിലും അതിൻ്റെ ഘടനയിലും തീവ്രമായ ബാഷ്പീകരണം സംഭവിക്കുന്ന ഒരു ശാരീരിക പ്രക്രിയയാണിത്. പൂരിത നീരാവിയും വായുവും അടങ്ങുന്ന കുമിളകളുടെ രൂപവത്കരണമാണ് തിളപ്പിക്കുന്നതിൻ്റെ അടയാളങ്ങളിലൊന്ന്.
തിളയ്ക്കുന്ന പോയിൻ്റ് പോലുള്ള ഒരു ആശയത്തിൻ്റെ അസ്തിത്വം ശ്രദ്ധിക്കേണ്ടതാണ്. നീരാവി രൂപീകരണ നിരക്ക് സമ്മർദ്ദത്തെ ആശ്രയിച്ചിരിക്കുന്നു. അത് ശാശ്വതമായിരിക്കണം. ചട്ടം പോലെ, ദ്രാവകങ്ങളുടെ പ്രധാന സ്വഭാവം രാസ പദാർത്ഥങ്ങൾസാധാരണ അന്തരീക്ഷമർദ്ദത്തിൽ തിളയ്ക്കുന്ന പോയിൻ്റാണ്. എന്നിരുന്നാലും, ഈ പ്രക്രിയയെ ശബ്ദ തരംഗങ്ങളുടെ തീവ്രത, വായു അയോണൈസേഷൻ തുടങ്ങിയ ഘടകങ്ങളാൽ സ്വാധീനിക്കാവുന്നതാണ്.
വെള്ളം തിളയ്ക്കുന്ന ഘട്ടങ്ങൾ
ചൂടാക്കൽ പോലുള്ള ഒരു നടപടിക്രമത്തിനിടയിൽ നീരാവി തീർച്ചയായും രൂപപ്പെടാൻ തുടങ്ങും. തിളപ്പിക്കുന്നതിൽ 4 ഘട്ടങ്ങളിലൂടെ ദ്രാവകം കടന്നുപോകുന്നത് ഉൾപ്പെടുന്നു:
- ചെറിയ കുമിളകൾ പാത്രത്തിൻ്റെ അടിഭാഗത്തും അതിൻ്റെ ചുവരുകളിലും രൂപപ്പെടാൻ തുടങ്ങുന്നു. കണ്ടെയ്നർ നിർമ്മിച്ച മെറ്റീരിയലിലെ വിള്ളലുകൾ ഉയർന്ന താപനിലയുടെ സ്വാധീനത്തിൽ വികസിക്കുന്ന വായു അടങ്ങിയിരിക്കുന്നു എന്നതിൻ്റെ ഫലമാണിത്.
- കുമിളകൾ വോളിയം വർദ്ധിപ്പിക്കാൻ തുടങ്ങുന്നു, ഇത് ജലത്തിൻ്റെ ഉപരിതലത്തിലേക്ക് പൊട്ടിത്തെറിക്കുന്നു. എങ്കിൽ മുകളിലെ പാളിദ്രാവകം ഇതുവരെ തിളയ്ക്കുന്ന പോയിൻ്റിൽ എത്തിയിട്ടില്ല, അറകൾ അടിയിലേക്ക് മുങ്ങുന്നു, അതിനുശേഷം അവ വീണ്ടും മുകളിലേക്ക് പരിശ്രമിക്കാൻ തുടങ്ങുന്നു. ഈ പ്രക്രിയ ശബ്ദ തരംഗങ്ങളുടെ രൂപീകരണത്തിന് കാരണമാകുന്നു. അതുകൊണ്ടാണ് വെള്ളം തിളയ്ക്കുമ്പോൾ ശബ്ദം കേൾക്കുന്നത്.
- ഉപരിതലത്തിലേക്ക് ഒഴുകുന്നു ഏറ്റവും വലിയ സംഖ്യകുമിളകൾ, ഇത് മതിപ്പ് സൃഷ്ടിക്കുന്നു, ഇതിനുശേഷം, ദ്രാവകം വിളറിയതായി മാറുന്നു. പരിഗണിച്ച് വിഷ്വൽ ഇഫക്റ്റ്, തിളയ്ക്കുന്ന ഈ ഘട്ടത്തെ "വൈറ്റ് കീ" എന്ന് വിളിക്കുന്നു.
- തീവ്രമായ സീതിംഗ് നിരീക്ഷിക്കപ്പെടുന്നു, ഇത് പെട്ടെന്ന് പൊട്ടിത്തെറിക്കുന്ന വലിയ കുമിളകളുടെ രൂപവത്കരണത്തോടൊപ്പമുണ്ട്. ഈ പ്രക്രിയ സ്പ്ലാഷുകളുടെ രൂപത്തോടൊപ്പമുണ്ട്, അതുപോലെ തന്നെ തീവ്രമായ നീരാവി രൂപീകരണവും.

ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക ചൂട്
മിക്കവാറും എല്ലാ ദിവസവും തിളയ്ക്കുന്നത് പോലെയുള്ള ഒരു പ്രതിഭാസത്തെ നാം അഭിമുഖീകരിക്കുന്നു. ബാഷ്പീകരണത്തിൻ്റെ പ്രത്യേക താപം ആണ് ഭൗതിക അളവ്, ഇത് താപത്തിൻ്റെ അളവ് നിർണ്ണയിക്കുന്നു. അതിൻ്റെ സഹായത്തോടെ, ഒരു ദ്രാവക പദാർത്ഥത്തെ നീരാവിയാക്കി മാറ്റാം. ഈ പരാമീറ്റർ കണക്കാക്കാൻ, നിങ്ങൾ ബാഷ്പീകരണത്തിൻ്റെ താപത്തെ പിണ്ഡം കൊണ്ട് ഹരിക്കേണ്ടതുണ്ട്.
അളക്കൽ എങ്ങനെയാണ് നടക്കുന്നത്?
ഉചിതമായ പരീക്ഷണങ്ങൾ നടത്തി ലബോറട്ടറി സാഹചര്യങ്ങളിൽ നിർദ്ദിഷ്ട സൂചകം അളക്കുന്നു. ഇവയിൽ ഇനിപ്പറയുന്നവ ഉൾപ്പെടുന്നു:
- അളന്നു ആവശ്യമായ തുകദ്രാവകം, അത് പിന്നീട് കലോറിമീറ്ററിലേക്ക് ഒഴിക്കുന്നു;
- ജലത്തിൻ്റെ താപനിലയുടെ പ്രാരംഭ അളവ് നടത്തുന്നു;
- മുമ്പ് സ്ഥാപിച്ച ടെസ്റ്റ് പദാർത്ഥമുള്ള ഒരു ഫ്ലാസ്ക് ബർണറിൽ ഇൻസ്റ്റാൾ ചെയ്തിട്ടുണ്ട്;
- പരീക്ഷണ പദാർത്ഥം പുറത്തുവിടുന്ന നീരാവി കലോറിമീറ്ററിലേക്ക് വിക്ഷേപിക്കുന്നു;
- ജലത്തിൻ്റെ താപനില വീണ്ടും അളക്കുന്നു;
- കലോറിമീറ്റർ തൂക്കിയിരിക്കുന്നു, ഇത് ബാഷ്പീകരിച്ച നീരാവിയുടെ പിണ്ഡം കണക്കാക്കാൻ അനുവദിക്കുന്നു.

ബബിൾ തിളപ്പിക്കൽ മോഡ്
തിളപ്പിക്കൽ എന്താണ് എന്ന ചോദ്യവുമായി ഇടപെടുമ്പോൾ, അതിന് നിരവധി മോഡുകൾ ഉണ്ടെന്ന് ശ്രദ്ധിക്കേണ്ടതാണ്. അങ്ങനെ, ചൂടാക്കുമ്പോൾ, നീരാവി കുമിളകളുടെ രൂപത്തിൽ രൂപം കൊള്ളുന്നു. അവ ഇടയ്ക്കിടെ വളരുകയും പൊട്ടിത്തെറിക്കുകയും ചെയ്യുന്നു. ഈ തിളപ്പിക്കൽ വ്യവസ്ഥയെ ന്യൂക്ലിയേറ്റ് തിളപ്പിക്കൽ എന്ന് വിളിക്കുന്നു. സാധാരണഗതിയിൽ, നീരാവി നിറച്ച അറകൾ പാത്രത്തിൻ്റെ ചുവരുകളിൽ കൃത്യമായി രൂപം കൊള്ളുന്നു. അവ സാധാരണയായി അമിതമായി ചൂടാക്കപ്പെടുന്നതാണ് ഇതിന് കാരണം. ഈ ആവശ്യമായ അവസ്ഥതിളപ്പിക്കുന്നതിന്, അല്ലാത്തപക്ഷം വലിയ വലിപ്പത്തിൽ എത്താതെ കുമിളകൾ തകരും.

ഫിലിം തിളപ്പിക്കൽ മോഡ്
തിളയ്ക്കുന്നത് എന്താണ്? ഈ പ്രക്രിയ വിശദീകരിക്കാനുള്ള എളുപ്പവഴി ഒരു നിശ്ചിത ഊഷ്മാവിൽ ബാഷ്പീകരണം ആണ് നിരന്തരമായ സമ്മർദ്ദം. ബബിൾ മോഡ് കൂടാതെ, ഒരു ഫിലിം മോഡും ഉണ്ട്. ശക്തിപ്പെടുത്തുമ്പോൾ എന്നതാണ് അതിൻ്റെ സാരം ചൂടിന്റെ ഒഴുക്ക്വ്യക്തിഗത കുമിളകൾ സംയോജിപ്പിച്ച് പാത്രത്തിൻ്റെ ചുവരുകളിൽ ഒരു നീരാവി പാളി ഉണ്ടാക്കുന്നു. ഒരു നിർണായക സൂചകം എത്തുമ്പോൾ, അവ ജലത്തിൻ്റെ ഉപരിതലത്തിലേക്ക് കടന്നുപോകുന്നു. ഈ തിളപ്പിക്കൽ മോഡ് വ്യത്യസ്തമാണ്, പാത്രത്തിൻ്റെ മതിലുകളിൽ നിന്ന് ദ്രാവകത്തിലേക്കുള്ള താപ കൈമാറ്റത്തിൻ്റെ അളവ് ഗണ്യമായി കുറയുന്നു. ഇതേ നീരാവി പടമാണ് ഇതിന് കാരണം.
തിളയ്ക്കുന്ന താപനില
ചൂടാക്കിയ ദ്രാവകത്തിൻ്റെ ഉപരിതലത്തിൽ ചെലുത്തുന്ന മർദ്ദത്തിൽ തിളയ്ക്കുന്ന പോയിൻ്റിൻ്റെ ആശ്രിതത്വം ഉണ്ടെന്നത് ശ്രദ്ധിക്കേണ്ടതാണ്. അതിനാൽ, 100 ഡിഗ്രി സെൽഷ്യസിൽ ചൂടാക്കിയാൽ വെള്ളം തിളപ്പിക്കുമെന്ന് പൊതുവെ അംഗീകരിക്കപ്പെടുന്നു. എന്നിരുന്നാലും, അന്തരീക്ഷമർദ്ദം സാധാരണ (101 kPa) ആയി കണക്കാക്കിയാൽ മാത്രമേ ഈ സൂചകം ന്യായമായി കണക്കാക്കാൻ കഴിയൂ. ഇത് വർദ്ധിക്കുകയാണെങ്കിൽ, തിളപ്പിക്കൽ പോയിൻ്റും മുകളിലേക്ക് മാറും. ഉദാഹരണത്തിന്, ജനപ്രിയ പ്രഷർ കുക്കർ പാനുകളിൽ മർദ്ദം ഏകദേശം 200 kPa ആണ്. അങ്ങനെ, തിളയ്ക്കുന്ന പോയിൻ്റ് 20 പോയിൻ്റ് (20 ഡിഗ്രി വരെ) വർദ്ധിക്കുന്നു.
താഴ്ന്ന അന്തരീക്ഷമർദ്ദത്തിൻ്റെ ഉദാഹരണം പർവതപ്രദേശങ്ങളാണ്. അതിനാൽ, അവിടെ അത് വളരെ ചെറുതായതിനാൽ, ഏകദേശം 90 ഡിഗ്രി താപനിലയിൽ വെള്ളം തിളപ്പിക്കാൻ തുടങ്ങുന്നു. അത്തരം പ്രദേശങ്ങളിലെ താമസക്കാർക്ക് ഭക്ഷണം തയ്യാറാക്കാൻ കൂടുതൽ സമയം ചെലവഴിക്കേണ്ടിവരുന്നു. അതിനാൽ, ഉദാഹരണത്തിന്, ഒരു മുട്ട തിളപ്പിക്കാൻ, നിങ്ങൾ കുറഞ്ഞത് 100 ഡിഗ്രി വെള്ളം ചൂടാക്കേണ്ടതുണ്ട്, അല്ലാത്തപക്ഷം വെള്ള കട്ടപിടിക്കില്ല.
ഒരു പദാർത്ഥത്തിൻ്റെ തിളപ്പിക്കൽ പോയിൻ്റ് പൂരിത നീരാവി മർദ്ദത്തെ ആശ്രയിച്ചിരിക്കുന്നു. താപനിലയിൽ അതിൻ്റെ പ്രഭാവം വിപരീത അനുപാതത്തിലാണ്. ഉദാഹരണത്തിന്, 357 ഡിഗ്രി സെൽഷ്യസിൽ ചൂടാക്കുമ്പോൾ മെർക്കുറി തിളച്ചുമറിയുന്നു. പൂരിത നീരാവി മർദ്ദം 114 Pa മാത്രമാണെന്ന വസ്തുത ഇത് വിശദീകരിക്കാം (വെള്ളത്തിന് ഈ കണക്ക് 101,325 Pa ആണ്).

വ്യത്യസ്ത സാഹചര്യങ്ങളിൽ തിളപ്പിക്കുക
ദ്രാവകത്തിൻ്റെ അവസ്ഥയും അവസ്ഥയും അനുസരിച്ച്, തിളയ്ക്കുന്ന പോയിൻ്റ് ഗണ്യമായി വ്യത്യാസപ്പെടാം. ഉദാഹരണത്തിന്, ദ്രാവകത്തിൽ ഉപ്പ് ചേർക്കുന്നത് മൂല്യവത്താണ്. ക്ലോറിൻ, സോഡിയം അയോണുകൾ ജല തന്മാത്രകൾക്കിടയിൽ സ്ഥാപിച്ചിരിക്കുന്നു. അതിനാൽ, തിളപ്പിക്കുന്നതിന് കൂടുതൽ ഊർജ്ജവും അതനുസരിച്ച് കൂടുതൽ സമയവും ആവശ്യമാണ്. കൂടാതെ, അത്തരം വെള്ളം വളരെ കുറച്ച് നീരാവി ഉത്പാദിപ്പിക്കുന്നു.
വെള്ളം തിളപ്പിക്കാൻ കെറ്റിൽ ഉപയോഗിക്കുന്നു ജീവിത സാഹചര്യങ്ങള്. ശുദ്ധമായ ദ്രാവകം ഉപയോഗിച്ചാൽ, പിന്നെ താപനില ഈ പ്രക്രിയ 100 ഡിഗ്രിയാണ് സ്റ്റാൻഡേർഡ്. സമാനമായ സാഹചര്യങ്ങളിൽ, വാറ്റിയെടുത്ത വെള്ളം തിളച്ചുമറിയുന്നു. എന്നിരുന്നാലും, വിദേശ മാലിന്യങ്ങളുടെ അഭാവം കണക്കിലെടുക്കുമ്പോൾ ഇതിന് കുറച്ച് സമയമെടുക്കും.
തിളപ്പിക്കലും ബാഷ്പീകരണവും തമ്മിലുള്ള വ്യത്യാസം എന്താണ്?
വെള്ളം തിളയ്ക്കുമ്പോഴെല്ലാം അന്തരീക്ഷത്തിലേക്ക് നീരാവി പുറത്തുവിടുന്നു. എന്നാൽ ഈ രണ്ട് പ്രക്രിയകളും തിരിച്ചറിയാൻ കഴിയില്ല. അവ ബാഷ്പീകരണത്തിൻ്റെ രീതികൾ മാത്രമാണ്, അത് ചില വ്യവസ്ഥകളിൽ സംഭവിക്കുന്നു. അതിനാൽ, തിളപ്പിക്കൽ ആദ്യ തരത്തിലുള്ളതാണ്. നീരാവി പോക്കറ്റുകളുടെ രൂപീകരണം മൂലമുണ്ടാകുന്നതിനേക്കാൾ ഈ പ്രക്രിയ കൂടുതൽ തീവ്രമാണ്. ബാഷ്പീകരണ പ്രക്രിയ ജലത്തിൻ്റെ ഉപരിതലത്തിൽ മാത്രമായി സംഭവിക്കുന്നു എന്നതും ശ്രദ്ധിക്കേണ്ടതാണ്. തിളപ്പിക്കൽ ദ്രാവകത്തിൻ്റെ മുഴുവൻ അളവിനെയും ബാധിക്കുന്നു.

ബാഷ്പീകരണം എന്തിനെ ആശ്രയിച്ചിരിക്കുന്നു?
ഒരു ദ്രാവകമോ ഖരമോ വാതകാവസ്ഥയിലേക്ക് മാറ്റുന്ന പ്രക്രിയയാണ് ബാഷ്പീകരണം. ആറ്റങ്ങളുടെയും തന്മാത്രകളുടെയും ഒരു "ഫ്ലൈറ്റ്" ഉണ്ട്, ചില വ്യവസ്ഥകളുടെ സ്വാധീനത്തിൽ മറ്റ് കണങ്ങളുമായുള്ള ബന്ധം ദുർബലമാകുന്നു. ഇനിപ്പറയുന്ന ഘടകങ്ങൾ കാരണം ബാഷ്പീകരണ നിരക്ക് വ്യത്യാസപ്പെടാം:
- ദ്രാവക ഉപരിതല പ്രദേശം;
- പദാർത്ഥത്തിൻ്റെ താപനില, അതുപോലെ തന്നെ പരിസ്ഥിതി;
- തന്മാത്രകളുടെ ചലന വേഗത;
- പദാർത്ഥത്തിൻ്റെ തരം.
ചുട്ടുതിളക്കുന്ന വെള്ളത്തിൻ്റെ ഊർജ്ജം ദൈനംദിന ജീവിതത്തിൽ ആളുകൾ വ്യാപകമായി ഉപയോഗിക്കുന്നു. ഈ പ്രക്രിയ വളരെ സാധാരണവും പരിചിതവുമാണ്, അതിൻ്റെ സ്വഭാവത്തെയും സവിശേഷതകളെയും കുറിച്ച് ആരും ചിന്തിക്കുന്നില്ല. എന്നിരുന്നാലും, രസകരമായ നിരവധി വസ്തുതകൾ തിളപ്പിക്കലുമായി ബന്ധപ്പെട്ടിരിക്കുന്നു:
- കെറ്റിലിൻ്റെ ലിഡിൽ ഒരു ദ്വാരമുണ്ടെന്ന് എല്ലാവരും ശ്രദ്ധിച്ചിരിക്കാം, പക്ഷേ കുറച്ച് ആളുകൾ അതിൻ്റെ ഉദ്ദേശ്യത്തെക്കുറിച്ച് ചിന്തിക്കുന്നു. നീരാവി ഭാഗികമായി പുറത്തുവിടുന്നതിനാണ് ഇത് ചെയ്യുന്നത്. അല്ലെങ്കിൽ, സ്പൗട്ടിലൂടെ വെള്ളം തെറിച്ചേക്കാം.
- ഉരുളക്കിഴങ്ങ്, മുട്ട, മറ്റ് ഭക്ഷ്യ ഉൽപന്നങ്ങൾ എന്നിവ പാചകം ചെയ്യുന്ന കാലയളവ് ഹീറ്റർ എത്ര ശക്തമാണെന്നതിനെ ആശ്രയിക്കുന്നില്ല. ചുട്ടുതിളക്കുന്ന വെള്ളത്തിൽ എത്രനേരം തുറന്നുകിടന്നിരുന്നു എന്നതാണ് പ്രധാനം.
- തിളയ്ക്കുന്ന പോയിൻ്റ് പോലുള്ള ഒരു സൂചകം ശക്തിയെ ബാധിക്കില്ല. ചൂടാക്കൽ ഉപകരണം. ഇത് ദ്രാവകത്തിൻ്റെ ബാഷ്പീകരണ നിരക്കിനെ മാത്രമേ ബാധിക്കുകയുള്ളൂ.
- തിളപ്പിക്കൽ എന്നത് വെള്ളം ചൂടാക്കൽ മാത്രമല്ല. ഈ പ്രക്രിയ ദ്രാവകം മരവിപ്പിക്കുന്നതിനും കാരണമാകും. അതിനാൽ, തിളയ്ക്കുന്ന പ്രക്രിയയിൽ, പാത്രത്തിൽ നിന്ന് തുടർച്ചയായി വായു പമ്പ് ചെയ്യേണ്ടത് ആവശ്യമാണ്.
- ഏറ്റവും കൂടുതൽ ഒന്ന് നിലവിലെ പ്രശ്നങ്ങൾവീട്ടമ്മമാർക്ക് പാൽ "ഓടിപ്പോകും" എന്നതാണ്. അതിനാൽ, മോശമായ കാലാവസ്ഥയിൽ ഈ പ്രതിഭാസത്തിൻ്റെ അപകടസാധ്യത ഗണ്യമായി വർദ്ധിക്കുന്നു, ഇത് അന്തരീക്ഷമർദ്ദം കുറയുന്നു.
- ഏറ്റവും ചൂടേറിയ ചുട്ടുതിളക്കുന്ന വെള്ളം ആഴത്തിലുള്ള ഭൂഗർഭ ഖനികളിൽ നിന്ന് ലഭിക്കുന്നു.
- എഴുതിയത് പരീക്ഷണാത്മക ഗവേഷണംചൊവ്വയിൽ 45 ഡിഗ്രി സെൽഷ്യസ് താപനിലയിൽ വെള്ളം തിളച്ചുമറിയുന്നുവെന്ന് സ്ഥാപിക്കാൻ ശാസ്ത്രജ്ഞർക്ക് കഴിഞ്ഞു.

ഊഷ്മാവിൽ വെള്ളം തിളപ്പിക്കാൻ കഴിയുമോ?
ലളിതമായ കണക്കുകൂട്ടലുകളിലൂടെ, സ്ട്രാറ്റോസ്ഫിയർ തലത്തിൽ വെള്ളം തിളപ്പിക്കുമെന്ന് സ്ഥാപിക്കാൻ ശാസ്ത്രജ്ഞർക്ക് കഴിഞ്ഞു. സമാനമായ അവസ്ഥകൾ ഉപയോഗിച്ച് പുനർനിർമ്മിക്കാൻ കഴിയും വാക്വം പമ്പ്. എന്നിരുന്നാലും, സമാനമായ ഒരു പരീക്ഷണം ലളിതവും കൂടുതൽ ലൗകികവുമായ സാഹചര്യങ്ങളിൽ നടത്താം.
ഒരു ലിറ്റർ ഫ്ലാസ്കിൽ നിങ്ങൾ 200 മില്ലി വെള്ളം തിളപ്പിക്കേണ്ടതുണ്ട്, കണ്ടെയ്നർ നീരാവി നിറയ്ക്കുമ്പോൾ, അത് ദൃഡമായി അടച്ച് ചൂടിൽ നിന്ന് നീക്കം ചെയ്യണം. ക്രിസ്റ്റലൈസറിന് മുകളിൽ സ്ഥാപിച്ച ശേഷം, തിളയ്ക്കുന്ന പ്രക്രിയ അവസാനിക്കുന്നതുവരെ നിങ്ങൾ കാത്തിരിക്കേണ്ടതുണ്ട്. അടുത്തതായി, ഫ്ലാസ്ക് ഒഴിക്കുന്നു തണുത്ത വെള്ളം. ഇതിനുശേഷം, കണ്ടെയ്നറിൽ വീണ്ടും തീവ്രമായ തിളപ്പിക്കൽ ആരംഭിക്കും. കുറഞ്ഞ താപനിലയുടെ സ്വാധീനത്തിൽ, ഫ്ലാസ്കിൻ്റെ മുകൾ ഭാഗത്ത് സ്ഥിതിചെയ്യുന്ന നീരാവി ഇറങ്ങുന്നു എന്നതാണ് ഇതിന് കാരണം.














